文章信息
- 张帅, 黄燕萍, 赵国敏, 潘明珠
- ZHANG Shuai, HUANG Yan-ping, ZHAO Guo-min, PAN Ming-zhu
- 基于层层自组装技术的复合聚电解质及其应用研究进展
- Research progress in polyelectrolyte complexes based on layer-by-layer self-assembly technology and their applications
- 材料工程, 2020, 48(12): 12-23
- Journal of Materials Engineering, 2020, 48(12): 12-23.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2019.000763
-
文章历史
- 收稿日期: 2019-08-21
- 修订日期: 2020-07-23
聚电解质(polyelectrolytes,PEs)是一类分子链上带有可电离基团的高聚物,广泛存在于生物体和自然界中,如蛋白质、DNA等。根据所带电荷不同,聚电解质分为阳离子聚电解质、阴离子聚电解质和两性聚电解质。利用带相反电荷的聚电解质之间的静电作用,可以在溶液中缔合形成具有三维高分子结构的复合聚电解质(polyelectrolyte complex,PEC)。1949年,Fuoss等[1]明确提出“聚电解质”这一概念,同时指出阳离子聚电解质和阴离子聚电解质可以发生反应形成絮状沉淀物,即复合聚电解质。20世纪50年代,随着高分子科学的发展,一系列具有高线性电荷密度的合成聚电解质被开发出来。此后,有关复合聚电解质的形成、物理化学特性及其应用开始得到研究者们的关注。
复合聚电解质的形成会显著影响聚合物溶液的溶解度、流变性、浊度和导电性,并且形成的复合聚电解质能够响应周围环境的变化并具备相应的性能。学者们对此进行了大量的研究,并开发出一系列方法(溶液滴定法、电解质溶液直接混合法、三元溶液共沉淀法、层层自组装法)用于制备复合聚电解质。其中,基于固体表面交替吸附带有相反电荷的聚电解质或多电荷分子形成复合多层膜的层层自组装技术(layer-by-layer self-assembly,LBL)是20世纪90年代发展起来的简便、多功能界面超分子自组装技术。将LBL技术引入复合聚电解质,通过调控阴、阳离子聚电解质的种类和组装工艺,便可赋予复合聚电解质特殊的性质,使其在纳米反应器、基因/药物载体、生物传感器、纤维和织物阻燃等领域获得广泛的应用。本文综述并讨论了基于LBL技术的复合聚电解质形成机理、影响因素及应用。
1 基于LBL技术构筑复合聚电解质复合聚电解质的形成可以通过混合两种带有相反电荷的聚电解质水溶液来实现,在此过程中,聚电解质相互之间的静电作用起主导作用。图 1显示了复合聚电解质的形成过程:(1)初级复合物的形成。由于静电作用,两种带相反电荷的聚电解质混合后立即形成初级复合物,这个过程仅需10~20 s;(2)复合物链构象的调整。在此过程中会形成新的静电键或原本的聚合物链发生变化,这一过程通常需1~2 h;(3)复合物的聚集过程[2-4]。在聚电解质链段疏水基团相互作用主导下,大分子重新排列,复合物链倾向于生成有序规整结构,最终形成胶束[5]、囊泡[6]、蠕虫[7]、薄膜[8]等不同形态的复合聚电解质。
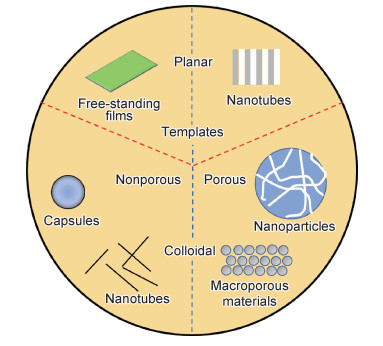
复合聚电解质得以层层自组装由以下两个因素决定:(1)阴、阳离子之间静电吸附形成离子对,使得游离态的聚电解质能够沉积到底膜;(2)电荷的过度补偿。当溶液中聚电解质沉积到底膜并中和底膜的相反电荷后,沉积过程不会直接停止,而是持续进行到底膜上聚电解质和溶液中聚电解质之间的静电排斥力足够大为止。早期研究中,受限于组装模板二维平面的结构,LBL技术多用于组装复合聚电解质膜。随着球形(带电胶体颗粒)和棒状(线性纳米管)模板的使用,LBL技术拓展至一维及三维领域,如图 2所示。
|
图 2 LBL模板示意图 Fig. 2 Schematic diagram of LBL templates |
平面模板LBL组装通常采用固体基板,如石英片、硅片和金属电极。具有特定孔结构的平面基板,如大孔膜,也被广泛用作LBL组装的模板。
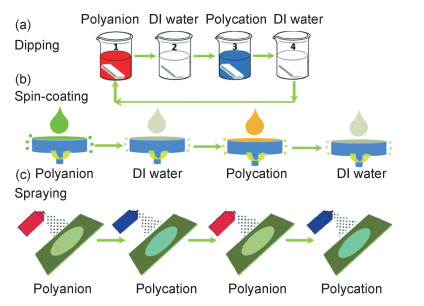
以平面模板为基底制备复合聚电解质的方法中(见图 3),交替浸涂法出现得最早,应用最为广泛(图 3(a))。然而,该方法组装步骤复杂,不适应工业化大规模生产。为此,学者们提出了一系列辅助LBL的技术以提高生产效率。2001年,Chiarelli等[9]将旋涂技术和静电组装技术相结合,分别以聚[1-[4-(3-羧基-4-羟基苯基偶氮)苯磺酰氨基]乙烷二基,钠盐]((poly[1-[4-(3-carboxy-4-hydroxyphenylazo)benzenesu lfonamido]-1, 2-ethanediyl], sodium salt), PAZO)和聚乙烯亚胺(polyethyleneimine, PEI)为原料,快速、高效地组装了聚电解质多层膜(图 3(b))。2005年,Decher等[10]以聚丙烯胺盐酸盐(poly(allylamine hydrochloride), PAH)和聚苯乙烯磺酸钠(poly(sodium-p-styrenesulfonate), PSS)为原料,采用交替喷涂技术制备出了PAH/PSS聚电解质多层膜(图 3(c)),组装速度较交替浸涂法提升了约25倍,为复合聚电解质的工业化应用打下了坚实的基础。
随着纳米技术的发展,一系列胶体模板,如聚苯乙烯(polystyrene, PS)、三聚氰胺甲醛树脂微粒(melamine-formaldehyde, MF)、碳纳米管(carbon nanotube, CNT)、碳酸钙(CaCO3)、纳米二氧化硅(SiO2)等被引入到聚电解质层层自组装过程中,实现了纳米尺度下复合聚电解质的自组装。Caruso等[12]分别以PS、MF微粒为模板,聚二烯丙基二甲基氯化铵(poly(diallyldimethylammonium chloride), PDDA)和SiO2为原料,通过LBL技术在模板表面组装了(PDDA/SiO2)多层膜。当组装3层时,膜的厚度为(110±10) nm。
以胶体颗粒为模板层层组装聚电解质微胶囊时,在沉积每层聚电解质之前均需要对组装颗粒进行清洗和离心操作,流程复杂,使得大规模制备聚电解质微胶囊耗时长、困难多。为此,Elizarova等[13]2016年提出了一种利用磷酸钙(Ca3(PO4)2)纳米粒子和管状流动式反应器来连续制备聚电解质微胶囊的方法。在管道中,模板粒子和聚电解质溶液混合,在模板上沉积一层聚电解质,随后,聚电解质粒子进入下一管道,与带相反电荷的聚电解质混合。重复上述过程,直到组装达到所需的层数。这种反应器具有每小时合成数十毫克微胶囊的潜力。
2 复合聚电解质的影响因素复合聚电解质的形成过程及性能受到阴、阳离子聚电解质电荷密度、pH值、离子强度、分子量、浓度等因素的影响。
2.1 电荷密度复合聚电解质的层层自组装是带有相反电荷的聚电解质之间静电吸附以及电荷过度补偿的过程,因此,电荷密度对聚电解质自组装过程存在极大的影响。
Schoeler等[14]较早地研究了电荷密度对阴、阳离子聚电解质交替沉积形成多层膜的影响。他们将具有匹配分子量的阳离子二甲基二烯丙基氯化铵(diallyldimethylammonium chloride, DADMAC)和N-甲基-N-乙烯基乙酰胺(N-Methyl-N-acetylethenamine, NMVA)的无规共聚物(DADMAC占比24%~100%)与PSS交替沉积成膜,并以电荷密度表示P(DADMAC-co-NMVA)共聚物中带电基团DADMAC所占比例。当电荷密度为53%~75%时,可以形成聚电解质多层膜,低于该范围无法形成多层膜,这一电荷密度称为临界电荷密度。此外,该研究还指出,不同电荷密度下表面形貌和吸附量存在联系。当超过临界电荷密度时,聚电解质电荷密度对P(DADMAC-co-NMVA)/PSS多层膜的厚度和粗糙度存在影响。高电荷密度下聚电解质以平面链参与组装形成光滑致密的薄膜,随着电荷密度下降,聚电解质形成环状或更为复杂的结构参与组装,复合膜表面结构也随之改变。
Lounis等[15]以聚赖氨酸(L-lysine, PLL)为阳离子聚电解质,丙烯酰胺(acrylamide, AM)与2-丙烯酰胺-2-甲基-1-丙磺酸(2-acrylamido-2-methylpropane sulfonic acid, AMPS)的共聚物(P(AM-co-AMPS))为阴离子聚电解质,研究了具有不同电荷密度的亲水性聚电解质之间的相互作用。改变P(AM-co-AMPS)的电荷密度(以带电基团AMPS占P(AM-co-AMPS)的百分比计)可以影响生成复合聚电解质的化学计量比。当电荷密度由15%提高至100%时,化学计量比由10提升到了70,同时电荷密度与两个带相反电荷的聚电解质之间的相互作用强度直接相关,电荷密度越高,相互作用强度也越大。浊度测量显示,当P(AM-co-AMPS)的化学电荷密度增大时,P(AM-co-AMPS)与PLL之间的静电相互作用增强,需要更高浓度的NaCl溶液才能使已经形成的复合聚电解质重新溶解。
2.2 pH值一般认为弱聚电解质中离子基团只有解离后才会与带有相反电荷的基团形成离子键。因此pH值对弱聚电解质存在较大影响,同时亦会影响复合聚电解质的形貌。
Joshi等[16]利用Zeta电位、浊度滴定和光散射测量等方法,研究了果胶与明胶A在pH=3~9范围内的络合反应。果胶在pH=3~9时带负电荷,明胶A在pH < 9时带正电荷。因此,当pH≤9时,聚电解质复合过程才可能发生,并且复合聚电解质随pH变化存在3个相转变点,从高到低分别为:pHc =9(结合开始)、pHφ=6.2(可溶性复合物的形成)和pHPrep=3(不溶性复合物的形成)。
Wasupalli等[17]报道了壳聚糖(chitosan, CS)和海藻酸钠(sodium alginate, AL)在室温下自组装形成复合聚电解质。在酸性条件(pH=3~7)下,复合聚电解质自组装形成纤维结构;pH值大于8时则会形成粒径在46~120 nm的纳米颗粒。Zhu等[18]则以CS和聚丙烯酸(polyacrylic acid, PAA)为原料,通过LBL技术制备了具有自愈合功能的复合聚电解质多层膜,并研究了pH对于CS/PAA聚电解质多层膜的影响。当CS溶液pH值为3.0时,聚电解质多层膜为网状结构,具备良好的溶胀性、亲水性和自愈合能力。
2.3 外加盐浓度外加盐会使得聚电解质链蜷缩,由舒展长链变为球状线团,从而以不同形态参与组装,进而影响组装膜的厚度及粗糙度。
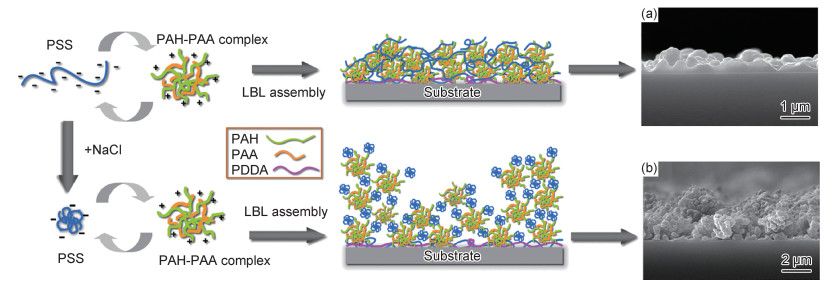
Grootha等[19]在中空纤维超滤膜上层层组装PDDA和PSS以制备纳滤膜。当NaCl浓度由0.005 mol/L提高至0.5 mol/L时,PDDA/PSS涂层厚度显著增加,纳滤膜渗透性提高。Zhang等[20]以带正电的复合聚电解质PAH/PAA和阴离子聚电解质PSS为原料,通过LBL法制备了聚电解质多层膜。如图 4所示,pH=9.3时,PAH/PAA构象不受NaCl浓度影响,PSS则随着NaCl浓度上升,分子构象由伸展逐渐趋于卷曲。当NaCl浓度由0 mol/L提高到2 mol/L,组装20层后,聚电解质多层膜由光滑变为粗糙,厚度也由(320±97) nm显著增加至(2±0.5) μm。Liu等[21]借助小振幅振荡剪切线性黏弹性测量研究了KBr对PSS/PDDA复合体系固-液相转化行为的影响,认为聚电解质复合过程中聚电解质链之间的“黏性”静电相互作用点可作为摩擦点,这些作用点受到溶液中离子强度的影响,进而可以调控材料的应力松弛行为。随着KBr浓度的提高,K+和Br-及水分子为PSS和PDDA分子链上的苯磺酸基和季铵基提供非本征电荷补偿,使得两种带有相反电荷的基团不再直接产生静电相互作用,从而破坏原本PSS/PDDA复合聚电解质内部的静电作用,使制备出的复合聚电解质重新溶解。这一KBr驱动的固-液转变的描述与Rouse模型关于黏度的解释相符。
|
图 4 (PSS0/PAH-PAA9)和(PSS2/PAH-PAA9.3)的LBL组装工艺的示意图和横截面扫描电镜图像 (膜沉积层数为20,在PSS溶液中有0 mol/L(a)和2 mol/L(b)NaCl)[20] Fig. 4 Schematic illustration and cross-sectional SEM images of the LBL assembly process of PSS0/PAH-PAA9.3 and PSS2/PAH-PAA9.3 films (the number of film deposition cycles is 20, with 0 mol/L(a) and 2 mol/L(b) NaCl in PSS solution[20]) |
最近,Kienle等[22]使用全内荧光(TIRF)显微镜研究了NaCl溶液对PLL/聚(2-丙烯酰胺-2-甲基-1-丙磺酸)(poly(2-acrylamido-2-methylpropane sulfonic acid), PAMPS)聚电解质多层膜中阳离子聚电解质PLL的横向迁移情况的影响。对PLL轨迹的分析表明,其运动行为为非电性的亚扩散运动,受到PLL/PAMAS多层膜黏弹性的影响。与以往对聚合物扩散的宏观测量相比,其微观扩散速度提高了2~3个数量级,并且与NaCl溶液浓度呈非单调变化。这一反常的扩散趋势归因于复合聚电解质薄膜黏弹性的盐依赖特性。在低盐浓度情况下,随NaCl浓度增加(0~0.5 mol/L),聚电解质薄膜收缩变硬,黏弹性降低,继续提高NaCl浓度,薄膜将膨胀软化,黏弹性提高,由盐浓度变化引起的聚电解质黏弹性变化进一步影响了PLL在聚电解质多层膜中的扩散运动。
3 复合聚电解质的形成机理为了精确地描述复合聚电解质形成过程,学者们进行了大量有益探索。基于Bungenberg de Jong的实验结果[23],Overbeek等[24]忽略体系中分子体积相互作用,假设复合聚电解质体系中的溶剂分子、聚电解质分子及抗衡离子具有相同的体积,最早提出了聚电解质复合理论,即Voorn-Overbeek(VO)理论。
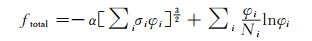
|
(1) |
式中:σi,φi,Ni分别代表聚电解质的电荷密度,体积分数及聚合度;α为与媒介有关的常数。系统总的自由能ftotal被表达成包含一个Debye-Hückel项(链上电荷与抗衡离子间的静电相互作用)和Flory-Huggins参数项(熵)的方程形式。该理论较好地解释了早期的实验结果,并对复合聚电解质相分离进行了简单推论。
VO理论认为聚电解质复合过程中,静电作用起主导作用,因此复合聚电解质的层层自组装需满足一定电荷要求时才能发生。然而,Vies等[25]发现具有不同等离子pH值(pH=5,9)的明胶间可以发生络合,此时VO理论已不再适用。为此他们提出了以熵驱动的聚电解质复合理论,即Veis-Aranyi(VA)理论:静电引力引起聚电解质自发聚集,形成固体和中性聚电解质微聚集体,随后这些聚集体在熵驱动下重新排列形成复合聚电解质。
随着聚电解质的发展,一系列具有高电荷密度及规则结构的聚电解质被合成。Spruijt等[26]以PAA和聚甲基丙烯酸N, N-二甲基氨基乙酯(poly(N, N-dimethylaminoethyl methacrylate), PDMAEMA)为原料,详细研究了聚电解质复合过程中相行为的变化,发现存在一临界盐浓度ϕSR。低于ϕSR时,复合聚电解质宏观下表现为相分离,形成稀薄的上清液和致密的沉淀。在PAA浓度ϕ=1 mol/L时,随着KCl浓度的增加,复合聚电解质在上清液中浓度增加,沉淀相内部浓度降低,沉淀相ϕc和上清液ϕs中的聚合物浓度逐渐接近,直到沉淀相溶解,溶液中复合聚电解质浓度均一为止。随着聚电解质分子量上升,临界盐浓度也有显著提升。其结果与早期VO理论预测一致。
Lu等[27]在VO理论基础上,以聚-L-赖氨酸盐酸盐(poly(l-lysine hydrochloride), PLK)和聚-D-L-谷氨酸钠(poly(d, l-glutamic acid), PRE)为原料,借助分子动态/蒙特卡罗(MD/MC)手段模拟了聚电解质复合过程。在反应过程中,NaCl优先分配到上清液相而非沉淀相中,且盐分配系数(沉淀相和上清液中盐浓度的比值)随着NaCl浓度的增加,由1逐渐下降至0.7,随后再次上升至1(临界盐浓度)。这一趋势受到体系中各种分子体积相互作用的强烈影响。该发现弥补了早期VO和VA理论中忽略聚电解质分子间体积相互作用的不足。
目前,以静电作用驱动的VO理论及熵驱动的VA理论能够在一定程度上解释聚电解质复合过程中相变化机制,但仍存在各自的适用范围,关于复合聚电解质形成的理论仍待进一步研究。
4 自组装复合聚电解质的应用 4.1 纳米反应器近年来,金属、半导体和磁性材料的无机纳米粒子由于量子局限效应和大比表面积特性而迅速发展成为一种具有突出性能的先进材料。这些纳米粒子在催化、电磁、光学方面受到极大的关注。为了有效操控和加工纳米颗粒,在大多数情况下,它们会被嵌入聚合物基体、聚合物薄膜或独立薄膜中。直接混合纳米粒子与聚合物是一种简单的策略,但该方法得到的复合材料往往具有不均匀的结构。为了获得有序、均匀的纳米颗粒膜,复合聚电解质常被用于负载纳米颗粒制备适宜的纳米反应器。利用LBL技术组装聚电解质并负载催化载体,可以制备具有不同结构及功能的纳米反应器,满足人们的崭新需求。
通过聚电解质层层自组装法制备的聚电解质多层膜已被用于负载Au,Ag,Pt和Pd等单金属纳米粒子以及Au-Ag合金纳米粒子制备纳米反应器。张信等[28]发展了一种基于聚电解质多层膜中的抗衡离子实现薄膜功能化的方法,通过抗衡离子交换/原位还原,在聚电解质多层膜中负载了Ag,Pt纳米粒子,使得复合薄膜具有良好抗菌性能和催化性能;并通过连续的阴离子交换/原位还原和阳离子交换/原位还原过程,合成了具有良好的催化效果的Au@Ag核壳纳米粒子。他们还以PDDA和PSS为构筑单元,选择AuCl4-和PtCl62-作为Au和Pt的前驱体,采取连续的阴离子交换/原位还原方法在聚电解质多层膜中依次引入Au和Pt的前驱体并原位还原,制备了Au@Pt核壳纳米粒子[29]。这类负载纳米粒子的聚电解质膜在电化学催化、燃料电池方面具有潜在的应用价值。
Kulkarni等[30]利用聚电解质的静电吸附作用制备了具有多层结构的纳米复合膜,氧化石墨烯(graphene oxide, GO)在聚电解质膜上定向排列使得材料的力学性能要明显高于GO无规则排列的复合膜。此外,聚电解质还可以充当GO的还原剂,溶解在溶液中的聚电解质在将GO还原的同时也可以改善石墨烯在溶液中的分散。
以H2和O2直接合成过氧化氢(H2O2)为例,该反应显示出了双金属纳米粒子(如Au-Pd,Pt-Pd,Sn-Pd等)在催化反应方面的巨大潜力。但考虑到H2在O2中的爆炸极限为4%~94%,实际催化反应中H2与O2只能以极低的浓度混合,使这一技术受到了严重的限制。为了解决这一问题,Kanungo等[31]以硅化毛细管为模板,选用了两种聚电解质PAA和PEI在毛细管内壁层层组装了聚电解质多层膜,并通过NaBH4还原法在PAA/PEI聚电解质多层膜表面原位还原了HAuCl4和K2PdCl4,而后通过煅烧除去聚电解质多层膜以构建Au-Pd双金属纳米反应器,并将该纳米反应器用于催化H2和O2直接制备H2O2。通过调控聚电解质多层膜的合成条件可以很容易地控制金属纳米粒子的负载量,而不会影响负载颗粒的尺寸。相较于传统的催化方法,该方法可以有效提高H2,O2的混合比(混合体积比50:50),并能显著提高催化效率,催化产率达到210 mol/(kg·h)。
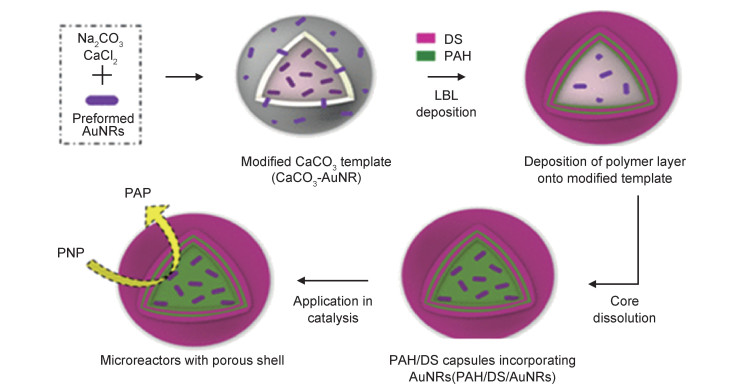
Sharma等[32]报告了一种将金纳米棒(AuNRs)和金纳米双锥(AuBPs)封装到聚电解质微胶囊中用于催化应用的策略。如图 5所示,他们在预装载AuNRs或AuBPs的CaCO3表面连续沉积PAH和硫酸葡聚糖(dextran sulfate, DS),随后脱除CaCO3模板制备了聚电解质微胶囊。制备出的聚电解质微胶囊成功地封装了尺寸为25~30 nm的AuNRs或AuBPs,且这些纳米颗粒在微胶囊内部均匀稳定分布。他们进一步研究在NaBH4存在下,以NRs,BPs为催化剂,将对硝基苯酚(p-nitrophenol, PNP)还原为对氨基苯酚(4-aminophenol, PAP)的催化效果。研究估算了微胶囊的反应顺序、转化率和速率常数等参数,并与悬浮状态下的未经封装的AuNRs或AuBPs微粒进行了比较。经微胶囊封装后,AuNRs及AuBPs的催化效率显著提高。同时,与BPs相比,NRS反应速率更高。
在医药领域,为了减少给药次数,降低药物不良反应,提高药物的生物利用度,许多药物需要经过合适的载体负载以达到药物缓释的目的。通过LBL法制备得到的聚电解质微胶囊具有尺寸可控、囊壁材料可选择范围广、较容易引入功能性基团而赋予微胶囊智能响应等优点,在药物缓释领域具有巨大的潜力。
如图 6所示,根据聚电解质微胶囊模板的差异,在微胶囊中封装药物颗粒的方式可分为3类:(1)预成型微胶囊载药;(2)药物晶体模板组装微胶囊载药;(3)多孔材料载药封装微胶囊[33]。
如图 6(a)所示,由于聚电解质微胶囊对于外部条件存在响应,因此将微胶囊置于药物溶液中,通过调节溶液pH、盐浓度等条件,使微胶囊打开小孔,当药物分子的大小/分子量允许其通过胶囊孔时,药物便可扩散到微胶囊中实现药物负载。基于CS/AL的多层胶囊常被用于设计刺激性反应药物递送载体。Cuomo等[34-37]较早以CS/AL层层组装脂质体核制备了pH响应性中空微胶囊。这些微胶囊可用作低分子量(罗丹明B)或高分子量(荧光素标记葡聚糖,Dextran-FITC,20,40,70 kDa)亲水性分子的药物载体,而微胶囊的渗透性则受到微胶囊厚度的影响,与沉积层数密切相关。
Li等[38]报道了将聚甲基丙烯酸(polymethacrylic acid, PMAA)纳米凝胶包裹在CS/AL多层微胶囊中制备生物相容性核壳微胶囊的方法,详细研究了PMAA纳米凝胶交联度和CS/AL微胶囊厚度对双嘧达莫负载和释放性能的影响。采用双层CS/AL pH响应型核壳微胶囊对疏水性抗癌药物阿霉素进行体外控释。研究结果指出,核-壳(PMAA@(CS/AL)n)聚电解质微胶囊是设计pH响应性控制药物递送系统的一种潜在平台。Ji等[39]通过LBL技术在纳米SiO2表面层层组装果胶和CS并通过去除纳米SiO2得到了果胶/CS聚电解质微胶囊,该微胶囊在磷酸缓冲盐溶液中96 h内具有良好的胶态稳定性,在牛血清白蛋白溶液中48 h内具有良好的胶态稳定性。同时,该胶囊对盐酸阿霉素具有较高的载药量和pH敏感性。体外抗癌活性实验表明,载药微胶囊能有效地杀伤人肝癌细胞(HepG2)。由于其对酸碱度的敏感性、良好的胶体稳定性和抗癌活性,此种聚电解质微胶囊作为一种新型的抗癌药物载体具有很大的潜力。尽管如此,受限于药物溶液的浓度,预成型微胶囊载药量受到限制。制备微胶囊的过程中,为了脱除模板,往往需要使用酸或某些有机溶剂处理微胶囊,可能会对微胶囊的活性有所损害。同时为了实现载药,微胶囊“打开”和“闭合”过程中所需的pH及盐浓度条件对于某些药物来说过于极端,因此该方法存在较大的限制。
4.2.2 药物晶体模板组装微胶囊载药当负载药物可以形成药物晶体的情况下,则直接以药物晶体模板组装微胶囊载药(图 6(b))。常见的药物主要有布洛芬[40-41]、吲哚美辛[42-44]、呋塞米[45-46]等。Qiu等[40]在尺寸为5~40 μm的布洛芬微晶表面层层组装CS,CS硫酸盐、羧甲基纤维素(carboxymethyl cellulose, CMC)或AL,组装膜层厚度20~60 μm。模拟实验显示,布洛芬在pH=1.4模拟胃液中释放缓慢,在pH=7.4的模拟肠液中快速溶解释放。同样,Ye等[43]采用LBL在5~10 μm的吲哚美辛微晶表面依次沉积AL和CS,其表面电荷相应转变为-41,+20 mV,表明了聚电解质膜层的形成。Santos等[41]以布洛芬为药物模板,借助超声辅助法层层组装了PAH/PSS聚电解质微胶囊,组装层数为7.5层时,微胶囊粒径为(127.5±38.0) nm,聚合物分散性指数(polymer dispersity index, PDI)为0.24,Zeta电位为(+32.7±0.6) mV,在水溶液中具有良好的胶体稳定性,体外细胞MTT(四唑盐)比色法测试表明该微胶囊具有生物相容性。根据组装层数不同,微胶囊可以在5~168 h内实现布洛芬的缓释。以药物晶体为模板,最大的优势是可以实现高的载药浓度,缺点则在于药物晶体在交替组装过程中会有较大的损失(组装10层后损失率>50%),且该方法要求负载药物能够形成晶体。
4.2.3 多孔材料载药封装微胶囊如图 6(c)所示,该方法是目前最通用的技术,使用较多的载药模板有CaCO3,PS,CNT,MF及纳米SiO2等。Balabushevich等[47]以CaCO3微粒为模板,通过吸附或共合成预先将药物(过氧化氢酶、胰岛素、抑肽酶)负载到CaCO3微粒中,随后以载药CaCO3微粒为模板层层组装DS/硫酸鱼精蛋白制备载药聚电解质微胶囊。与预成型微胶囊封装药物相比,多孔模板预封装能够提高微胶囊的载药量(过氧化氢酶含量可由70 mg/g提高至630 mg/g),且微胶囊内蛋白的生物活性不受聚电解质多层膜相互作用的影响。该研究有助于将脆弱的生物大分子封装到聚电解质微胶囊中,明显拓展了复合聚电解质在生物医药领域的应用前景。
4.3 生物传感器生物传感器是一类以酶、抗体等生物活性物质作为敏感元件,配上适当的换能器,通过生物分子与被测物的特异生物反应而发挥检测和定量测定功能的工具,因其具有操作简单、成本低、性能优异、响应速度快、连续性好等优点被作为一种新型的检测手段应用于临床。聚电解质层层自组装过程常常以水为介质,反应条件温和并且可以同时装配几种生物材料,这一特点使其在生物传感器领域得到了广泛的应用。
Kreft等[48]制备了封装有活体细胞染料SNARF-1-葡聚糖偶联物的PSS/PAH多层膜和磁性纳米颗粒的聚电解质微胶囊用作可移动的pH传感器。以成纤维细胞和乳腺癌细胞为例,SNARF-1具有pH响应的荧光基团,微胶囊在培养基碱性条件下发出红色荧光,被细胞摄取后在细胞内酸性条件下发出绿色荧光,在摄取微胶囊过程中细胞仍保持其生存和分裂增殖的能力。制备出的生物传感器能够测量信号清晰的各种类型细胞的生理参数。这一简单的构筑策略是LBL聚电解质微胶囊作为生物传感器检测物理生物参数的先驱性工作之一。
Piccinini等[49]在还原石墨烯氧化物场效应晶体管(rGO-FET)表面层层自组装了PEI和尿素酶用于检测尿素,该传感器借助了液体门控制石墨烯晶体管的pH依赖性,通过测量尿素催化水解中局部的pH变化来检测尿素。他们使用叉指微通道以降低晶体管噪声、提高pH灵敏度(20.3 μA/pH)和跨导值(800 μS)。研究者们进一步采用弱聚电解质PEI/尿素酶对rGO-FET进行改性,借助静电门控效应改善晶体管的pH响应性。在尿素环境下,由于尿素酶的催化水解,石墨烯表面附近的pH值发生变化,rGO-FET显示出狄拉克点移动。该生物传感器能在低电压(小于500 mV)下运行,并且检测限低(1 μmol/L),能够在1~1000 μmol/L范围内监测尿素,具有响应快,稳定性好的特点。
多巴胺的测定能够提供生物学功能的重要信息,并有可能成为评估如帕金森病的重要的病理条件。Zhao等[50-51]报道了在玻碳电极(GCE)上组装PDDA和多壁碳纳米管(MWNT)聚电解质多层膜作为抗坏血酸(Vitamin C)存在条件下多巴胺的检测工具。当检测环境中存在Vitamin C时,未经处理的玻碳电极无法区分多巴胺和尿酸的电化学信号,但在电极上组装PDDA/MWNT聚电解质膜后便能分别获得多巴胺和尿酸清晰的电化学伏安信号。因此,聚电解质层层自组装法可用于简单、快速地订制电极,用以检测生物流体中的特定代谢物含量。
酶是一种多功能的生物催化剂,具有广泛的催化和传感应用,聚电解质微胶囊常被用来负载酶制备生物传感器。Kazakova等[52]制备了PAH/PSS微胶囊,并在其中分别封装葡萄糖氧化酶(glucose oxidase, GOD)、乳酸氧化酶或GOD/乳酸氧化酶的复合物,将其用于制备比色生物传感器。PSS分别用三(4, 7-联苯-1, 10-邻菲啰啉)二氯化钌(Ru(dpp))和二氢罗丹明123(DHR123)标记。激发波长为488 nm时,Ru(dpp)发出红色荧光(波长560~700 nm);非荧光分子DHR123在过氧化物酶的存在条件下会与过氧化氢(H2O2)反应产生罗丹明123(R123),发出绿色荧光(波长510~600 nm)。根据荧光强度对氧、葡萄糖和乳酸进行浓度依赖的荧光光谱分析,发现荧光强度与葡萄糖及乳酸浓度呈线性关系,在毫摩尔范围内显示可靠的检测结果。Antipina等[53]提出了在一个平台上进行多次葡萄糖检测的策略。他们采用纳米压印光刻技术对乙烯-四氟乙烯共聚物(ETFE)基体进行改性,制备了1.2 mm的微孔。这些微孔起到了PAH/PSS微胶囊的锚定点的作用,微胶囊由于重力和毛细管力而被包裹在微孔中。去核后,将GOD和辣根过氧化物酶(POD)装入微胶囊中,随后向ETFE基体表面滴加葡萄糖和荧光试剂(Amplex Red),葡萄糖与GOD反应产生H2O2,H2O2进一步与POD反应将电子供体Amplex Red转化为强荧光物质试卤灵,在激光扫描共聚焦显微镜下出现荧光。采用这一策略,微胶囊可以借助于化学手段固定在非特定载体上用于检测微量化学物质。使用上述生物传感器,病人可以在家中方便快速地进行疾病筛查,而无需任何特殊的手术训练。鉴于LBL器件在生物传感方面的潜力,随着技术进步,生物传感器的小型化将进一步获得发展。
4.4 纤维及织物阻燃利用聚电解质在高分子材料表面组装形成阻燃涂层的这一新型阻燃方法,由于具有高阻燃效率、良好的环境可接受性及对聚合物性能影响较小的特点而受到了学者们的广泛关注[54]。
聚电解质层层自组装法阻燃技术在天然织物如棉、麻织物阻燃方面极具优越性,并且以含磷聚电解质构成涂层可以获得更好的阻燃效果。目前主流的阻燃方法主要是利用成炭/膨胀系统及纳米颗粒涂层两种方法。前者常用一些含磷聚电解质如聚磷酸铵(ammonium polyphosphate, APP)、植酸(phytic acid, PA)、磷酸纤维素等与带有相反电荷的聚电解质结合从而在燃烧过程中生成稳定的炭层。常用的带相反电荷的聚电解质包括CS、PEI、木质素磺酸钠等。而后者则利用经过处理的无机纳米粒子组装到阻燃基体表面形成具有阻隔作用的涂层。
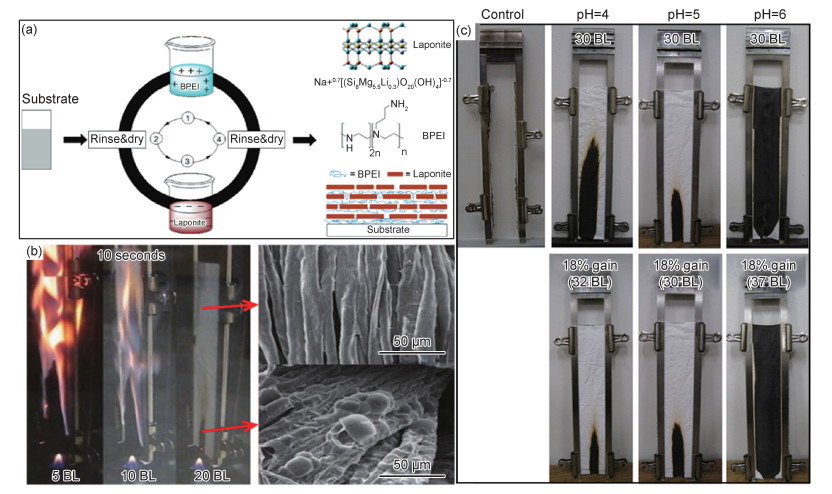
Srikulkit等[55]最早于2006年报道了复合聚电解质在阻燃领域的应用。他们将CS和聚磷酸(polyphosphoric acid, PPA)层层自组装到丝绸表面,利用氮、磷的协同作用在单个丝纤维的外部形成凝聚相成炭涂层,用以改善材料的热稳定性。组装30层CS/PPA后,材料在600 ℃下的残炭量达到40%,然而报道中未涉及实际的燃烧实验。受到LBL法特点的启发,Li等[56]于2009年利用该技术在棉织物表面构建了锂藻土/支化PEI(BPEI)聚电解质多层膜(图 7(a)),提高了基体的热稳定性和阻燃性能。随后多种多样的自组装方法出现在了织物阻燃领域。
Li等[57]选用PAH和聚磷酸钠(poly(sodium phosphate), PSP)等两种聚电解质在棉织物表面构建了一种在热解过程中增强成炭性能的LBL膨胀型聚电解质阻燃涂层,该阻燃剂以PAH为气源,PSP为酸源,纤维素为炭源,使得棉织物在垂直火焰测试(VFT)期间可以实现自熄(图 7(b))。该涂层建立了纤维素纤维多层阻燃剂的标准,并且在降低热释放速率和实现自熄性能方面是最有效的阻燃涂料之一。
|
图 7 LBL工艺制备锂藻土/BPEI示意图[56](a),涂有20层的PAH/PSP涂层的棉织物自熄[57](b)和无涂层,以不同的pH水平沉积30层CS/PA(上)和沉积18%(质量分数)的CS/PA(下)的织物的图像[58](c) Fig. 7 Schematic diagrams of the LBL deposition process used to prepare Laponite/BPEI assemblies[56](a), cotton self-extinguishing with a 20 bilayer coating of PAH/PSP[57](b) and images of uncoated control and fabrics coated with 30 bilayer of CS-PA (top) and 18%(mass fraction)CS/PA (bottom) deposited at varying pH level[58] (c) |
Laufer等[58]利用两种环境友好且可再生的聚电解质CS和PA在棉织物表面构建膨胀型涂层,该涂层在垂直火焰测试中表现出与PAH/PSP涂层相似的自熄特性(图 7(c))。微型量热仪的峰值放热率(pkHRR)和总放热率(THR)分别显著降低了60%和76%。
Zhang等[59]在苎麻织物表面构建了PEI/APP聚电解质阻燃涂层,阻燃织物在垂直火焰实验中表现出自熄和膨胀行为,在电子显微镜下观察到炭层气泡。Pan等[60]以甲醛、三聚氰胺和硫酸氢钠为原料,在水溶液中合成了磺化三聚氰胺甲醛(sulfonated melamine-formaldehyde, SMF)树脂。以阴离子聚电解质SMF为发泡剂,结合CS和PA,采用LBL自组装技术在棉织物表面制备膨胀型阻燃涂层,成功地在棉纤维表面沉积了(CS/SMF+PA)n涂层。与纯棉相比,棉织物在400~700 ℃下的热稳定性有所提高。700 ℃氮气氛围下,组装5层和10层的棉织物的残炭量分别比纯棉织物提高了25.9%和32%。在垂直火焰实验中,组装10层可实现织物自熄。
为了充分利用可再生资源,一系列天然聚电解质材料被引入到自组装复合聚电解质阻燃领域中。Alongi等[61]将脱氧核糖核酸与CS组装到棉织物表面,在燃烧过程中同样可以形成膨胀型涂层,使基体自熄且热释放速率降低了40%。Pan等[62-63]合成了多种磷化生物质聚电解质如磷酸纤维素、磷酸化壳聚糖等并将其与生物质聚电解质通过层层自组装在棉织物表面形成全生物质的涂层,同样可以使基体自熄并非常有效地降低其热释放速率。利用LBL技术构建复合聚电解质阻燃涂层是迄今为止对天然纤维最有效的阻燃处理方法之一。
受限于LBL技术,聚电解质阻燃往往局限在棉、麻织物、聚乳酸薄膜等平面材料。进一步拓展阻燃聚电解质的应用范围已成为现今研究的一大热点。最近,Koklukaya等[64]采用LBL技术,将阳离子聚电解质PEI和阴离子聚电解质六偏磷酸钠(sodium hexametaphosphate, SHMP)组成的聚电解质多层膜吸附到纤维素纤维上,以提高纤维纸的阻燃性和拉伸强度,并采用聚电解质滴定法研究了不同分子量PEI对纤维素纤维和CMC的吸附情况。纤维经PEI和SHMP连续处理,表面沉积3.5层复合聚电解质,处理后的纤维用于制备纸张。此外,他们还制备了一种湿强度纸,并用相同的LBL涂层对其进行处理。纤维的起始热解温度降低,800 ℃下的残留量增加。使用高分子量PEI/SHMP经LBL组合处理的纤维素和CMC制备的纸张,尽管吸附的聚电解质量相当少,但它们形成了非常薄的薄膜(湿厚度约17 nm),与未经处理的纤维素纤维相比,组装3.5层高分子量PEI/SHMP使纸张的断裂应力增加了100%。
5 结束语复合聚电解质在众多领域具有广泛的应用前景,并且在纳米反应器、药物缓释、生物传感器、纤维织物阻燃等领域已经得到了实际的应用,许多具有特定功能的聚电解质也相继被研发出来。但目前自组装复合聚电解质的制备方法仍主要局限于LBL法及其衍生而来的一系列方法。这些方法尽管行之有效,却不可避免地提高了复合聚电解质的应用成本。与此同时,随着学者们对复合聚电解质研究的不断深入,对复合聚电解质形成过程的理论研究更加透彻,对于拟制备的复合聚电解质也提出了更高的要求。
当今及未来复合聚电解质的研究热点仍将关注于以下几点:(1)简化复合聚电解质的组装工艺,降低生产成本,使其满足工业化大规模生产的需求;(2)利用聚电解质对外界环境的响应性精确控制聚电解质结构和形态;(3)实现复合聚电解质的多功能化,通过对组装工艺的设计以及对于聚电解质材料的选择与调控,制备多功能复合聚电解质。
| [1] |
FUOSS R M, SADEK H. Mutual interaction of polyelectrolytes[J]. Science, 1949, 110(2865): 552-554. DOI:10.1126/science.110.2865.552 |
| [2] |
GÄRDLUND L, WÅGBERG L, GERNANDT R. Polyelectrolyte complexes for surface modification of wood fibres: Ⅱ influence of complexes on wet and dry strength of paper[J]. Colloids & Surfaces A Physicochemical & Engineering Aspects, 2003, 218(1): 137-149. |
| [3] |
GÄRDLUND L, WÅGBERG L, NORGREN M. New insights into the structure of polyelectrolyte complexes[J]. Journal of Colloid & Interface Science, 2007, 312(2): 237-246. |
| [4] |
DOBRYNIN A V, COLBY R H, RUBINSTEIN M. Scaling theory of polyelectrolyte solutions[J]. Macromolecules, 1996, 28(6): 1859-1871. |
| [5] |
HARADA A, KATAOKA K. Formation of polyion complex micelles in an aqueous milieu from a pair of oppositely-charged block copolymers with poly(ethylene glycol) segments[J]. Macromolecules, 1995, 28(15): 5294-5299. DOI:10.1021/ma00119a019 |
| [6] |
CHUANOI S, KISHIMURA A, DONG W F, et al. Structural factors directing nanosized polyion complex vesicles (nano-PICsomes) to form a pair of block aniomer[sol] homo catiomers: studies on the aniomer segment length and the catiomer side-chain structure[J]. Polymer Journal, 2015, 46(2): 130-135. |
| [7] |
WIBOWO A, OSADA K, MATSUDA H, et al. Morphology control in water of polyion complex nanoarchitectures of double-hydrophilic charged block copolymers through composition tuning and thermal treatment[J]. Macromolecules, 2014, 47(9): 267-275. |
| [8] |
RICHARDSON J J, BJÖRNMALM M, CARUSO F. Technology-driven layer-by-layer assembly of nanofilms[J]. Science, 2015, 348(6233): aaa2491-1-aaa2491-11. |
| [9] |
CHIARELLI P A, JOHAL M S, CASSON J L, et al. Controlled fabrication of polyelectrolyte multilayer thin films using spin-assembly[J]. Advanced Materials, 2001, 13(15): 1167-1171. DOI:10.1002/1521-4095(200108)13:15<1167::AID-ADMA1167>3.0.CO;2-A |
| [10] |
IZQUIERDO A, ONO S S, VOEGEL J C, et al. Dipping versus spraying: exploring the deposition conditions for speeding up layer-by-layer assembly[J]. Langmuir the ACS Journal of Surfaces & Colloids, 2005, 21(16): 7558-7567. |
| [11] |
XIAO F X, PAGLIARO M, XU Y J, et al. Layer-by-layer assembly of versatile nanoarchitectures with diverse dimensionality: a new perspective for rational construction of multilayer assemblies[J]. Chemical Society Reviews, 2016, 45(11): 3088-3121. DOI:10.1039/C5CS00781J |
| [12] |
CARUSO F, CARUSO R A, MÖHWALD H. Production of hollow microspheres from nanostructured composite particles[J]. Chemistry of Materials, 1999, 11(11): 3309-3314. DOI:10.1021/cm991083p |
| [13] |
ELIZAROVA I S, LUCKHAM P F. Fabrication of polyelectrolyte multilayered nano-capsules using a continuous layer-by-layer approach[J]. Journal of Colloid & Interface Science, 2016, 470: 92-99. |
| [14] |
SCHOELER B, KUMARASWAMY G, CARUSO F. Investigation of the influence of polyelectrolyte charge density on the growth of multilayer thin films prepared by the layer-by-layer technique[J]. Macromolecules, 2002, 35(3): 889-897. DOI:10.1021/ma011349p |
| [15] |
LOUNIS F M, CHAMIEH J, LECLERCQ L, et al. Interactions between oppositely charged polyelectrolytes by isothermal titration calorimetry: effect of ionic strength and charge density[J]. Journal of Physical Chemistry: B, 2017, 121(12): 2684-2694. DOI:10.1021/acs.jpcb.6b11907 |
| [16] |
JOSHI N, RAWAT K, BOHIDAR H B. pH and ionic strength induced complex coacervation of Pectin and Gelatin A[J]. Food Hydrocolloids, 2018, 74: 132-138. DOI:10.1016/j.foodhyd.2017.08.011 |
| [17] |
WASUPALLI G K, VERMA D. Molecular interactions in self-assembled nano-structures of chitosan-sodium alginate based polyelectrolyte complexes[J]. International Journal of Biological Macromolecules, 2018, 114: 10-17. DOI:10.1016/j.ijbiomac.2018.03.075 |
| [18] |
ZHU Y, XUAN H, REN J, et al. Self-healing multilayer polyelectrolyte composite film with chitosan and poly(acrylic acid)[J]. Soft Matter, 2015, 11(43): 8452-8459. DOI:10.1039/C5SM01463H |
| [19] |
GROOTH J D, OBORNY R, POTRECK J, et al. The role of ionic strength and odd-even effects on the properties of polyelectrolyte multilayer nanofiltration membranes[J]. Journal of Membrane Science, 2015, 475: 311-319. DOI:10.1016/j.memsci.2014.10.044 |
| [20] |
ZHANG L, GUO H, SUN J. Salt effects on the structural tailoring of layer-by-layer assembled polyelectrolyte complexes and salt-containing polyelectrolyte films[J]. Thin Sold Films, 2018, 653: 258-266. DOI:10.1016/j.tsf.2018.03.048 |
| [21] |
LIU Y, MOMANI B, WINTER H H, et al. Rheological characterization of liquid-to-solid transitions in bulk polyelectrolyte complexes[J]. Soft Matter, 2017, 13(40): 7332-7340. DOI:10.1039/C7SM01285C |
| [22] |
KIENLE D F, SCHWARTZ D K. Complex salt dependence of polymer diffusion in polyelectrolyte multilayers[J]. Journal of Physical Chemistry Letters, 2019, 10(5): 987-992. DOI:10.1021/acs.jpclett.9b00004 |
| [23] |
BUNGENBERG DE JONG H G, KRUYT H R. Coacervation (partial miscibility in colloid systems)[J]. Proceedings of the Koninklijke Nederlandse Akademie Van Wetenschappen, 1929, 32: 849-856. |
| [24] |
OVERBEEK J T, VOORN M J. Phase separation in polyelectrolyte solutions. theory of complex coacervation[J]. Journal of Cellular Physiology, 1957, 49(Suppl 1): 7-22. |
| [25] |
VEIS A, ARANYI C. Phase separation in polyelectrolyte systems. Ⅰ. complex coacervates of gelatin[J]. Journal of Chemical Physics, 1960, 64: 1203-1210. DOI:10.1021/j100838a022 |
| [26] |
SPRUIJT E, WESTPHAL A H, BORST J W, et al. Binodal compositions of polyelectrolyte complexes[J]. Plant Cell Reports, 2010, 15(12): 905-909. |
| [27] |
LU L, SRIVASTAVA S, ANDREEV M, et al. Phase behavior and salt partitioning in polyelectrolyte complex coacervates[J]. Macromolecules, 2018, 51(8): 2988-2995. DOI:10.1021/acs.macromol.8b00238 |
| [28] |
张信, 储诚灿, 黄凯华, 等. 以聚电解质多层膜为纳米反应器制备Au@Pt核壳纳米粒子[J]. 应用化学, 2012, 29(12): 1433-1437. ZHANG X, CHU C C, HUANG K H, et al. Preparation of Au@Pt core-shell nanoparticles using polyelectrolyte multilayers as nanoreactors[J]. Chinese Journal of Applied Chemistry, 2012, 29(12): 1433-1437. DOI:10.3969/j.issn.1001-4160.2012.12.006 |
| [29] |
ZHANG X, ZAN X, SU Z. Polyelectrolyte multilayer supported Pt nanoparticles as catalysts for methanol oxidation[J]. Journal of Materials Chemistry, 2011, 21(44): 17783-17789. DOI:10.1039/c1jm12892b |
| [30] |
KULKARNI D D, CHOI I, SINGAMANENI S S, et al. Graphene oxide-polyelectrolyte nanomembranes[J]. ACS Nano, 2010, 4(8): 4667-4676. DOI:10.1021/nn101204d |
| [31] |
KANUNGO S, PAUNOVIC V, SCHOUTEN J C, et al. Facile synthesis of catalytic AuPd nanoparticles within capillary microreactors using polyelectrolyte multilayers for the direct synthesis of H2O2[J]. Nano Letters, 2017, 17(10): 6481-6486. DOI:10.1021/acs.nanolett.7b03589 |
| [32] |
SHARMA V, SUNDARAMURTHY A. Reusable hollow polymer microreactors incorporated with anisotropic nanoparticles for catalysis application[J]. ACS Omega, 2019, 4(1): 628-636. DOI:10.1021/acsomega.8b02820 |
| [33] |
JOHNSTON A P R, CORTEZ C, ANGELATOS A S, et al. Layer-by-layer engineered capsules and their applications[J]. Current Opinion in Colloid & Interface Science, 2006, 11(4): 203-209. |
| [34] |
CUOMO F, LOPEZ F, MIGUEL M G, et al. Vesicle-templated layer-by-layer assembly for the production of nanocapsules[J]. Langmuir, 2010, 26(13): 10555-10560. DOI:10.1021/la100584b |
| [35] |
CUOMO F, LOPEZ F, CEGLIE A, et al. pH-responsive liposome-templated polyelectrolyte nanocapsules[J]. Soft Matter, 2012, 8(16): 4415-4420. DOI:10.1039/c2sm07388a |
| [36] |
CUOMO F, CEGLIE A, PILUDU M, et al. Loading and protection of hydrophilic molecules into liposome-templated polyelectrolyte nanocapsules[J]. Langmuir, 2014, 30(27): 7993-7999. DOI:10.1021/la501978u |
| [37] |
CUOMO F, LOPEZ F, PILUDU M, et al. Release of small hydrophilic molecules from polyelectrolyte capsules: effect of the wall thickness[J]. Journal of Colloid & Interface Science, 2015, 447: 211-216. |
| [38] |
LI X, DU P, LIU P. Layer-by-layer polyelectrolyte complex coated poly(methacrylic acid) nanogels as a drug delivery system for controlled release: structural effects[J]. RSC Advances, 2014, 4(99): 56323-56331. DOI:10.1039/C4RA05066E |
| [39] |
JI F, LI J, QIN Z, et al. Engineering pectin-based hollow nanocapsules for delivery of anticancer drug[J]. Carbohydr Polym, 2017, 177: 86-96. DOI:10.1016/j.carbpol.2017.08.107 |
| [40] |
QIU X P, LEPORATTI S, DONATH E, et al. Studies on the drug release properties of polysaccharide multilayers encapsulated ibuprofen microparticles[J]. Langmuir, 2001, 17(17): 5375-5380. DOI:10.1021/la010201w |
| [41] |
SANTOS A C, PATTEKARI P, JESUS S, et al. Sonication-assisted layer-by-layer assembly for low solubility drug nanoformulation[J]. ACS Applied Materials & Interfaces, 2015, 7(22): 11972-11983. |
| [42] |
MIRGORODSKAYA A B, KUSHNAZAROVA R A, NIKITINA A V, et al. Polyelectrolyte nanocontainers: controlled binding and release Chook for of indomethacin[J]. Journal of Molecular Liquids, 2018, 271: 982-989. |
| [43] |
YE S, WANG C, LIU X, et al. Deposition temperature effect on release rate of indomethacin microcrystals from microcapsules of layer-by-layer assembled chitosan and alginate multilayer films[J]. Journal of Controlled Release, 2005, 106(3): 319-328. DOI:10.1016/j.jconrel.2005.05.006 |
| [44] |
DALMORO A, SITENKOV A Y, LAMBERTI G. Ultrasonic atomization and polyelectrolyte complexation to produce gastroresistant shell-core microparticles[J]. Journal of Applied Polymer Science, 2016, 133(6): 42976. |
| [45] |
RADWAN S E, SOKAR M S, ABDELMONSIF D A, et al. Mucopenetrating nanoparticles for enhancement of oral bioavailability of furosemide: in vitro and in vivo evaluation/sub-acute toxicity study[J]. International Journal of Pharmaceutics, 2017, 526(1): 366-379. |
| [46] |
STRYDOM S J, OTTO D P, STIEGER N, et al. Self-assembled macromolecular nanocoatings to stabilize and control drug release from nanoparticles[J]. Powder Technology, 2014, 256(2): 470-476. |
| [47] |
BALABUSHEVICH N G, GUERENU A V L D, FEOKTISTOVA N A, et al. Protein-containing multilayer capsules by templating on mesoporous CaCO3 particles: post- and pre-loading approaches[J]. Macromolecular Bioscience, 2016, 16(1): 95-105. DOI:10.1002/mabi.201500243 |
| [48] |
KREFT O, JAVIER A M, SUKHORUKOV G B, et al. Polymer microcapsules as mobile local pH-sensors[J]. Journal of Materials Chemistry, 2007, 17(42): 4471-4476. DOI:10.1039/b705419j |
| [49] |
PICCININI E, BLIEM C, REINER-ROZMAN C, et al. Enzyme-polyelectrolyte multilayer assemblies on reduced graphene oxide field-effect transistors for biosensing applications[J]. Biosensors & Bioelectronics, 2016, 92: 661-667. |
| [50] |
ZHAO W, XU J J, CHEN H Y. Extended-range glucose biosensor via layer-by-layer assembly incorporating gold nanoparticles[J]. Frontiers in Bioscience: A, 2005, 10: 1060-1069. DOI:10.2741/1599 |
| [51] |
WEI Z, XU J J, CHEN H Y. Electrochemical biosensors based on layer-by-layer assemblies[J]. Electroanalysis, 2010, 18(18): 1737-1748. |
| [52] |
KAZAKOVA L I, SHABARCHINA L I, ANASTASOVA S, et al. Chemosensors and biosensors based on polyelectrolyte microcapsules containing fluorescent dyes and enzymes[J]. Analytical & Bioanalytical Chemistry, 2013, 405(5): 1559-1568. |
| [53] |
ANTIPINA M N, KIRYUKHIN M V, CHONG K, et al. Patterned microcontainers as novel functional elements for microTAS and LOC[J]. Lab on A Chip, 2009, 9(10): 1472-1475. DOI:10.1039/b819725c |
| [54] |
MALUCELLI G. Layer-by-layer nanostructured assemblies for the fire protection of fabrics[J]. Materials Letters, 2016, 166: 339-342. DOI:10.1016/j.matlet.2015.12.103 |
| [55] |
SRIKULKIT K, IAMSAMAI C, DUBAS S T. Development of flame retardant polyphosphoric acid coating based on the polyelectrolyte multilayers technique[J]. J Metals Mater Miner, 2006, 16(2): 5-41. |
| [56] |
LI Y C, SCHULZ J, GRUNLAN J C. Polyelectrolyte/nanosilicate thin-film assemblies: influence of pH on growth, mechanical behavior, and flammability[J]. ACS Appl Mater Interfaces, 2009, 1(10): 2338-2347. DOI:10.1021/am900484q |
| [57] |
LI Y C, MANNEN S, MORGAN A B, et al. Intumescent all-polymer multilayer nanocoating capable of extinguishing flame on fabric[J]. Advanced Materials, 2011, 23(34): 3926-3931. DOI:10.1002/adma.201101871 |
| [58] |
LAUFER G, KIRKLAND C, MORGAN A B, et al. Intumescent multilayer nanocoating, made with renewable polyelectrolytes, for flame-retardant cotton[J]. Biomacromolecules, 2012, 13(9): 2843-2848. DOI:10.1021/bm300873b |
| [59] |
TAO Z, YAN H, WANG L, et al. Controlled formation of self-extinguishing intumescent coating on ramie fabric via layer-by-layer assembly[J]. Industrial & Engineering Chemistry Research, 2013, 52(18): 6138-6146. |
| [60] |
PAN Y, ZHAO H. A novel blowing agent polyelectrolyte for fabricating intumescent multilayer coating that retards fire on cotton fabric[J]. Journal of Applied Polymer Science, 2018, 135(32): 46583. DOI:10.1002/app.46583 |
| [61] |
ALONGI J, CAROSIO F, MALUCELLI G. Influence of ammonium polyphosphate-/poly(acrylic acid)-based layer by layer architectures on the char formation in cotton, polyester and their blends[J]. Polymer Degradation & Stability, 2012, 97(9): 1644-1653. |
| [62] |
PAN H, SONG L, MA L, et al. Layer-by-layer assembled thin films based on fully biobased polysaccharides: chitosan and phosphorylated cellulose for flame-retardant cotton fabric[J]. Cellulose, 2014, 21(4): 2995-3006. DOI:10.1007/s10570-014-0276-5 |
| [63] |
PAN H, WANG W, PAN Y, et al. Formation of self-extinguishing flame retardant biobased coating on cotton fabrics via layer-by-layer assembly of chitin derivatives[J]. Carbohydrate Polymer, 2015, 115: 516-524. DOI:10.1016/j.carbpol.2014.08.084 |
| [64] |
KÖKLVKAYA O, CAROSIO F, WÅGBERG L. Tailoring flame-retardancy and strength of papers via layer-by-layer treatment of cellulose fibers[J]. Cellulose, 2018, 25(4): 2691-2709. DOI:10.1007/s10570-018-1749-8 |
 2020, Vol. 48
2020, Vol. 48